Häufige Irrtümer: Desinfektionsreinigung in kontrollierten Umgebungen
Wichtige Erkenntnisse:
- Daten aus der Umweltüberwachung (EM) sind nicht immer ein zuverlässiger Indikator für das Kontaminationsrisiko, da sie nur eine Momentaufnahme darstellen und möglicherweise nicht mit der tatsächlichen Produktexposition oder der Leistung aseptischer Prozesse korrelieren.
- Rückstände von Desinfektionsmitteln stellen nicht grundsätzlich ein Risiko für die Produktqualität dar und die Annahme, dass Rückstände lebensfähige Mikroorganismen beherbergen, ist wissenschaftlich nicht belegt. Das Rückstandsmanagement sollte daher auf einem risiko-orientierten Ansatz beruhen.
- Das Sprühen von Desinfektionsmitteln ist nicht automatisch besser als das Wischen oder das Reinigen mit dem Wischmopp, da die Wirksamkeit von der vollständigen Abdeckung der Oberfläche abhängt und die mechanische Wirkung des Wischens die Entfernung von Mikroben verbessern kann.
- Die routinemäßige Verwendung von Desinfektionsmitteln und Sporiziden ist für die Aufrechterhaltung der Reinraumkontrolle unerlässlich, jedoch sollten Annahmen hinsichtlich ihrer Leistungsgrenzen – wie beispielsweise die Entwicklung von Resistenzen oder die Beeinträchtigung durch Rückstände – kritisch hinterfragt werden.
- Strategien zur Desinfektionsmittelanwendung sollten auf die spezifischen Faktoren der Einrichtung zugeschnitten sein, darunter Oberflächentypen, Zugänglichkeit der Bereiche und bisherige Trends der Umweltüberwachung, anstatt sich auf allgemeine oder veraltete Praktiken zu verlassen.
Wenn es um Mikrobiologie geht, gibt es viele Irrtümer und Missverständnisse, von der „5-Sekunden-Regel“ für Lebensmittel, die auf den Boden gefallen sind, bis hin zu überlieferten „Weisheiten“, wie etwa dass man bei Erkältungen hungern und bei Fieber viel essen soll. Im Bereich der Reinraum- und pharmazeutischen Mikrobiologie haben sich einige „Irrtümer“ etabliert, die sogar von Aufsichtsbehörden bestätigt werden. Beispielsweise gibt es immer noch einige Behörden, die auf einer Rotation von Desinfektionsmitteln bestehen, um die Entwicklung resistenter Bakterienstämme zu verhindern. Die Autoren verfolgen hier das Ziel, mithilfe von Logik und fundierten wissenschaftlichen Erkenntnissen einige mikrobiologische Irrtümer im Zusammenhang mit der Desinfektionsreinigung kontrollierter Umgebungen zu widerlegen.
Einige der fragwürdigen Überzeugungen, Praktiken und Richtlinien, auf die wir gestoßen sind, sind nachfolgend aufgeführt:
IRRTUM: Daten aus der Umweltüberwachung (Environmental Monitoring, EM) sind ein zuverlässiger Indikator für Risiken hinsichtlich der Produktqualität.
TATSACHE: Verwertbare mikrobiologische Daten zur Umweltüberwachung spiegeln in der Regel eine Momentaufnahme wider und stellen einen vorübergehenden Zustand dar, der möglicherweise bestehen bleibt, aber nicht unbedingt. Ein einzelner Datenpunkt (d. h. eine Oberflächenprobe) kann nicht unbedingt über seine unmittelbaren Probenparameter hinaus als relevant extrapoliert werden. Die Autoren haben kontaminierte aseptische Prozesssimulationen (Medienfüllungen) beobachtet, bei denen die zugehörige Umweltüberwachung völlig sauber war (0 KBE). Umgekehrt haben wir einwandfreie Ergebnisse für eine Medienfüllung gesehen, bei der die zugehörigen Umweltüberwachungsdaten ungewöhnlich hohe Verunreinigungen und mehrere Überschreitungen der Warn- und Aktionsstufen zeigten. Die Interpretation von Daten zur Umweltüberwachung in Reinräumen ist eine sehr differenzierte Aufgabe, die am besten von gut ausgebildetem und erfahrenem Personal durchgeführt wird.
IRRTUM: Rückstände getrockneter Desinfektionsmittel auf Oberflächen stellen grundsätzlich ein Risiko für die Qualität von Arzneimitteln dar.
TATSACHE: Unter bestimmten Bedingungen können alle Arten von Rückständen auf der Oberfläche ein Qualitätsrisiko darstellen. Die Theorie, dass Desinfektionsmittelrückstände lebensfähige Mikroorganismen beherbergen können, ist eine unbewiesene Annahme und angesichts der Stoffwechselbedürfnisse lebensfähiger Mikroorganismen eher unlogisch. Ein risikobasierter und wissenschaftlich fundierter Ansatz zur Behandlung von Desinfektionsmittelrückständen oder anderen Reinraumrückständen ist die einzig empfehlenswerte Vorgehensweise.
IRRTUM: Durch das Aufsprühen von Desinfektionsmitteln auf Oberflächen wird im Vergleich zum Wischen oder Reinigen mit dem Wischmopp eine bessere Abdeckung und damit Wirksamkeit erreicht. TATSACHE: Auf die Technik kommt es an! Flüssige chemische Desinfektionsmittel wirken durch direkten Kontakt mit Zellmembranen. Das Sprühen kann wirksam sein, wenn die ganze Fläche abgedeckt wird. Die mechanische Wirkung des Wischens und des Reinigens mit dem Wischmopp hat ebenfalls Vorteile. Der Vergleich der beiden Methoden ist keine einfache oder eindeutige Angelegenheit. Unternehmen müssen viele Faktoren berücksichtigen, um die optimale Anwendungsmethode für ihre Prozesse und Anlagen zu bestimmen, darunter unter anderem: Oberflächenmaterialien und Komplexität, Größe und Zugänglichkeit der Bereiche sowie frühere Ergebnisse der Umweltüberwachung. Eine formelle Risikobewertung kann dabei helfen, die beste Vorgehensweise zu bestimmen.
IRRTUM: Um Schimmelpilze mithilfe von Umweltüberwachung vollständig zu beseitigen, muss eine Abhilfemaßnahme mit einem sporiziden Mittel auf der Oberfläche durchgeführt werden.
TATSACHE: Wie oben erwähnt, sind die Ergebnisse der Umweltüberwachung Momentaufnahmen und spiegeln in der Regel vorübergehende Zustände wider. Angesichts der Zeitspanne zwischen der Probenentnahme und dem Erhalt der Ergebnisse (normalerweise 3–5 Tage) haben in dem Bereich wahrscheinlich viele Aktivitäten stattgefunden, die es unlogisch machen, so zu reagieren, als seien die Bedingungen unverändert geblieben. Oftmals ist die betroffene Oberfläche bereits mit einem keimtötenden Reinigungsmittel mit fungizider Wirkung behandelt worden. Vorbeugen ist besser als nachträglich reagieren: Eine gründliche Untersuchung der Ursache des Schimmelpilzbefalls und die Verhinderung seines erneuten Auftretens ist ein besserer und wissenschaftlich fundierterer Ansatz.
Irrtum: Mehr ist besser
Bei zahlreichen Besuchen in biopharmazeutischen und medizintechnischen Einrichtungen haben die Autoren komplexe Verfahren zur Desinfektion von Reinraumoberflächen gesehen, bei denen drei oder mehr Arten von Desinfektionsmitteln und mehrere Arten von sporiziden Mitteln zum Einsatz kamen. Beispielsweise setzen eine Reihe von Unternehmen, die wir kürzlich in Südamerika besucht haben, solche komplexen Systeme ein. Diese komplizierten Ansätze zur Reinraumdesinfektion stellen eine Belastung für die Mitarbeitenden dar, die diese Aufgaben ausführen, ohne einen zusätzlichen Nutzen hinsichtlich der Kontrolle der Keimbelastung zu erzielen. Tatsache ist, dass die routinemäßige Verwendung eines einzigen keimtötenden Reinigungsmittels mit Breitbandwirkung in Verbindung mit der regelmäßigen und gezielten Anwendung eines sporiziden Mittels ein vollständig wirksames Programm darstellt, um in den meisten Reinraumumgebungen eine ausreichende Keimbelastungskontrolle zu erreichen1.
Frage: Wenn ein Sporizid alles tötet, sollten wir es dann nicht einfach immer verwenden?
Antwort: Die chemische Inaktivierung bakterieller Endosporen erfordert ziemlich aggressive Formulierungen, wie etwa Natriumhypochlorit oder Wasserstoffperoxid-PAA-Mischungen (Peressigsäure/Essigsäure). Eine zu häufige Verwendung von oxidierenden Sporiziden kann zu Korrosionsproblemen im Reinraum sowie zu Risiken für Umwelt, Gesundheit und Sicherheit führen. Daher sollten Sporizide umsichtig eingesetzt werden, wobei die Häufigkeit auf dem Risiko und den bisherigen Ergebnissen der Umweltüberwachung hinsichtlich endosporenbildender Bakterien basieren sollte.
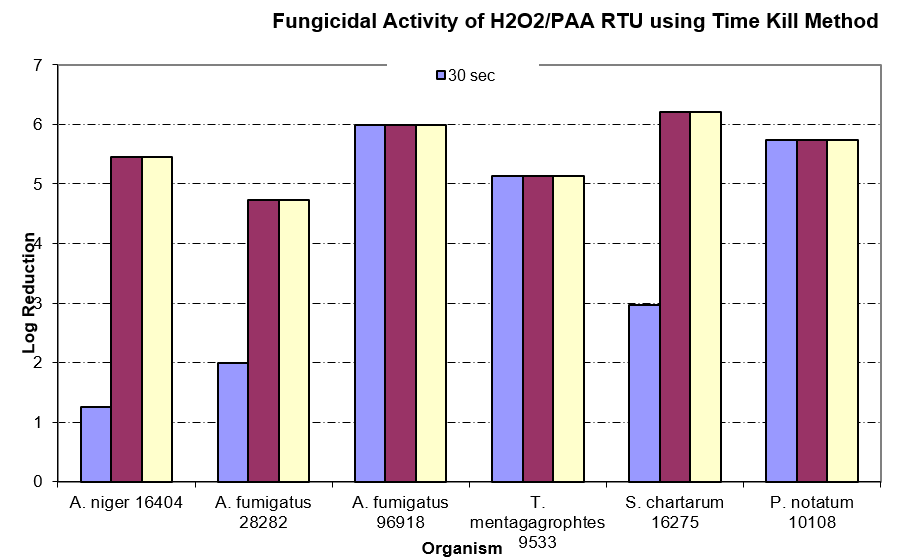
Alkohol ist ein weiteres Reinraummittel, das nicht immer richtig eingesetzt wird. Viele Einrichtungen verwenden für Gegenstände, die in die Reinraumumgebung gelangen, nur 70%igen IPA, weil sie davon ausgehen, dass er gegen Pilz- und Bakteriensporen wirksam ist. Es kann eine gewisse Wirkung auf Pilzsporen geben, wie in der folgenden Tabelle (Time-Kill-Studie2) zu sehen ist, aber um das Eindringen von Sporenbildnern in den Reinraum zu verhindern, ist ein echtes sporizides Mittel erforderlich.
Wirksamkeit von gebrauchsfertigem (RTU) Wasserstoffperoxid/Peressigsäure gegen Schimmelpilze
Häufig werden Benutzer gemäß Standardarbeitsanweisungen (SOP) darin geschult, mit flachen Wischmopps an Wänden und Böden in einer Richtung mit sich überschneidenden Bewegungen zu wischen. Diese Technik kann jedoch bei unzureichender Schulung und mangelnder Anwendung der richtigen Vorgehensweise zu Problemen führen. Die richtige Herstellung der Verdünnungen ist ein weiterer wichtiger Faktor für eine wirksame Desinfektion3. Messzylinder und Einzeldosispackungen sind die genaueste Methode. Es ist niemals ratsam, konzentriertes Desinfektionsmittel nach Augenmaß in einen Eimer zu gießen.
Ein wirksames Reinigungs- und Desinfektionsprogramm sollte immer ein Desinfektionsmittel mit Breitbandwirkung und ein Sporizid zur Bekämpfung bakterieller Endosporen im Reinraumbetrieb umfassen.

(Image Credit: http://www.pppmag.com/article/714/June_2010/Cleaning_Practices_for_Cleanroom_Contamination_Control/)
Irrtum: Desinfektionsmittelrückstände beherbergen eine Keimbelastung und beeinträchtigen die Wirksamkeit eines Sporizids
Zur Aufrechterhaltung der Umweltkontrolle in Reinräumen ist die routinemäßige Anwendung von Desinfektions- und Sporizidmitteln erforderlich. Bei regelmäßiger Verwendung dieser Produkte können Rückstände auf der Oberfläche zurückbleiben. Durch die Verwendung inkompatibler Chemikalien im Wechsel können Probleme auftreten, aber fördern Desinfektionsmittelrückstände allein die mikrobielle Kontamination? Und beeinträchtigen Desinfektionsmittelrückstände die sporizide Wirksamkeit?
Die Phenol-Desinfektionsmittel der nächsten Generation von STERIS wurden in einer Time-Kill-Studie auf Rückstände getestet, um die Auswirkungen auf die Wirksamkeit eines sporiziden Mittels (SporKlenz® RTU) im Vergleich zu Bacillus subtilis, ATCC-Nr. 19659 zu beurteilen. Die Feststoffe (µg/cm2) des getrockneten Desinfektionsmittels wurden in einer separaten Studie ermittelt. Dabei wurde die Rückstandsmenge nach mehreren Anwendungen auf einem 116 cm2 großen Teststreifen aus Edelstahl berechnet, um die typische Verwendung im Reinraum zu simulieren. Außerdem wurde die Menge an gebrauchsfertigem SporKlenz RTU berechnet, die zur Abdeckung einer Oberfläche bei typischen Anwendungen als Verdünnungsmittel erforderlich ist. Im letzteren Fall wurde festgestellt, dass 120 mg SporKlenz RTU Sterilisationsmittel für einen 116 cm2 großen Teststreifen ausreichten. Die in diesem Versuch ermittelten Verhältnisse wurden extrapoliert, um die Verdünnung der Desinfektionsmittelrückstände zu bestimmen, die in eine Lösung mit sporizidem Wirkstoff gegeben werden müssen.
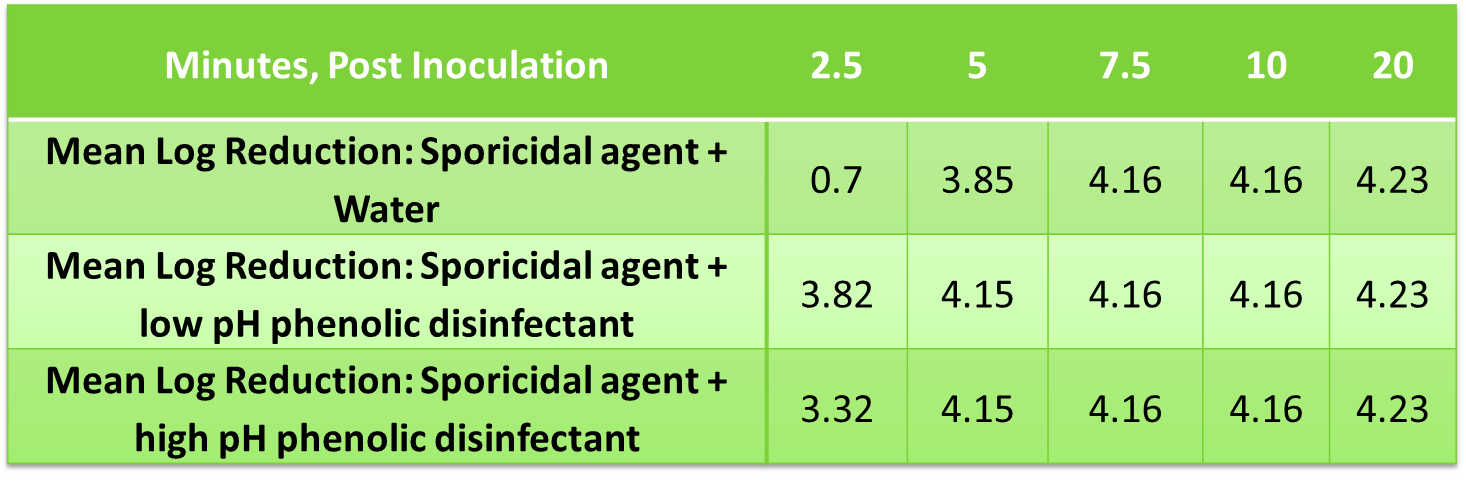
Ein Volumen von 0,1 ml der Mikroorganismensuspension wurde zu 9,9 ml der Testlösung (d. h. Spor-Klenz RTU Sterilisationsmittel, versetzt mit einem phenolhaltigen Desinfektionsmittel mit niedrigem oder hohem pH-Wert) gegeben. Eine Pufferkontrolle wurde mit derselben Menge versetzt. Nach der Inokulation wurde nach 2,5, 5, 7,5, 10 und 20 Minuten jeweils eine Probe von 0,1 ml entnommen. Die Proben wurden neutralisiert, plattiert und 48–49 Stunden lang bei 37 ± 2 °C inkubiert. Die lebensfähigen Organismen pro ml Probe wurden durch standardmäßige aerobe Plattenzählung bestimmt.
Mittlere Log-Reduktion von B. subtilis durch Verwendung von Phenolrückständen und einer sporiziden Wirkstofflösung
Irrtum: Desinfektionsmittelrückstände beherbergen eine Keimbelastung und beeinträchtigen die Wirksamkeit eines Sporizids
Zur Aufrechterhaltung der Umweltkontrolle in Reinräumen ist die routinemäßige Anwendung von Desinfektions- und Sporizidmitteln erforderlich. Bei regelmäßiger Verwendung dieser Produkte können Rückstände auf der Oberfläche zurückbleiben. Durch die Verwendung inkompatibler Chemikalien im Wechsel können Probleme auftreten, aber fördern Desinfektionsmittelrückstände allein die mikrobielle Kontamination? Und beeinträchtigen Desinfektionsmittelrückstände die sporizide Wirksamkeit?
Die Phenol-Desinfektionsmittel der nächsten Generation von STERIS wurden in einer Time-Kill-Studie auf Rückstände getestet, um die Auswirkungen auf die Wirksamkeit eines sporiziden Mittels (SporKlenz® RTU) im Vergleich zu Bacillus subtilis, ATCC-Nr. 19659 zu beurteilen. Die Feststoffe (µg/cm2) des getrockneten Desinfektionsmittels wurden in einer separaten Studie ermittelt. Dabei wurde die Rückstandsmenge nach mehreren Anwendungen auf einem 116 cm2 großen Teststreifen aus Edelstahl berechnet, um die typische Verwendung im Reinraum zu simulieren. Außerdem wurde die Menge an gebrauchsfertigem SporKlenz RTU berechnet, die zur Abdeckung einer Oberfläche bei typischen Anwendungen als Verdünnungsmittel erforderlich ist. Im letzteren Fall wurde festgestellt, dass 120 mg SporKlenz RTU Sterilisationsmittel für einen 116 cm2 großen Teststreifen ausreichten. Die in diesem Versuch ermittelten Verhältnisse wurden extrapoliert, um die Verdünnung der Desinfektionsmittelrückstände zu bestimmen, die in eine Lösung mit sporizidem Wirkstoff gegeben werden müssen.
Ein Volumen von 0,1 ml der Mikroorganismensuspension wurde zu 9,9 ml der Testlösung (d. h. Spor-Klenz RTU Sterilisationsmittel, versetzt mit einem phenolhaltigen Desinfektionsmittel mit niedrigem oder hohem pH-Wert) gegeben. Eine Pufferkontrolle wurde mit derselben Menge versetzt. Nach der Inokulation wurde nach 2,5, 5, 7,5, 10 und 20 Minuten jeweils eine Probe von 0,1 ml entnommen. Die Proben wurden neutralisiert, plattiert und 48–49 Stunden lang bei 37 ± 2 °C inkubiert. Die lebensfähigen Organismen pro ml Probe wurden durch standardmäßige aerobe Plattenzählung bestimmt.
Mittlere Log-Reduktion von B. subtilis durch Verwendung von Phenolrückständen und einer sporiziden Wirkstofflösung

Die Daten zeigen keine hemmenden/antagonistischen Effekte des getrockneten Rückstands auf die sporizide Wirksamkeit.
Grundlegende Schulung
Es ist eine bedauerliche Tatsache, dass in der Biopharmazie-, OSD- und Medizingerätebranche die „Reinigungsteams“, also diejenigen, die für die Desinfektion der regulierten Reinraumproduktionsbereiche verantwortlich sind, im Vergleich zu anderen Abteilungen (z. B. Qualitätskontrolle, Fertigung) oft am wenigsten Schulung, Anleitung und Aufsicht erhalten. Aus Kostengründen wird die Desinfektionsreinigung häufig einem Vertragsreinigungsunternehmen übertragen, was die Schulungsfragen noch komplizierter macht und das Reinigungspersonal der Qualitätskontrolle und -sicherung entzieht. Durch die Schichtarbeit ist es noch schwieriger, einen Überblick darüber zu erhalten, was in der Produktion vor sich geht. Auf dem heutigen globalen Markt müssen möglicherweise auch Sprachbarrieren überwunden werden. Noch komplizierter wird die Sache dadurch, dass die erfolgreiche Desinfektion von Reinraumoberflächen und -umgebungen vollständig von den Fähigkeiten und Techniken der Mitarbeitenden abhängt. Anders als bei der physischen Reinigung von sichtbarem Schmutz erscheinen Reinraumoberflächen normalerweise bereits sauber. Die Mitarbeitenden haben dann die Aufgabe, unsichtbare Stoffe zu entfernen, sei es lebensfähige Keimbelastung oder nicht sichtbare Partikelverunreinigungen. Es gibt kaum oder gar keine visuellen Hinweise darauf, wann eine Oberfläche wirksam dekontaminiert wurde. Aus diesen Gründen müssen die Mitarbeitenden, die die Desinfektionsreinigung durchführen, außergewöhnlich gut geschult sein und sich mit den Grundsätzen der Mikrobiologie, der Kontaminationskontrolle und der aseptischen Verfahren auskennen.
Referenzen:
- PDA Technical Report No. 70 (2015). Fundamentals of Cleaning and Disinfection Programs for Aseptic Manufacturing Facilities. Verfügbar bei Parenteral Drug Association, Inc.
- Polarine, J., Macauley, J., Karanja, P., Klein, D., Martin, A. (2009) Evaluating the Activity of Disinfectants Against Fungi. Cleanrooms: The Magazine of Contamination Control Technology 23(2).
- http://www.pppmag.com/article/714/June_2010/Cleaning_Practices_for_Cleanroom_Contamination_Control/
Vorgeschlagene Inhalte
Ein begründeter Prozess zur Reinigung und Desinfektion
Bewährte Verfahren für die Validierung von Desinfektionsmitteln in Reinräumen
Rückstandsentfernung in Reinräumen: Ein regulatorischer Überblick
Tragen Sie sich in unsere E-Mail-Liste ein, um die aktuellsten Branchennachrichten und Produkt-Updates zu erhalten.
Indem Sie auf „Abonnieren“ klicken, bestätigen Sie, dass Sie mit unseren allgemeinen Geschäftsbedingungen einverstanden sind.



